Anúncios
As empresas Pfizer e BioNTech entraram nesta terça-feira (1º) com pedido de autorização, nos Estados Unidos, para aplicar sua vacina contra a Covid-19 em crianças de 6 meses a 4 anos. A previsão da empresa é aplicar um esquema de três doses.
A agência regulatória de saúde dos EUA, a FDA (Food and Drug Administration), anunciou que fará, no próximo dia 15 de fevereiro, uma reunião para avaliar o pedido. A solicitação da empresa segue a modalidade “submissão contínua”, na qual os dados são enviados progressivamente para o órgão regulador.
Anúncios
Atualmente, Pfizer e BioNTe estão testando a eficácia de uma terceira dose do seu imunizante para esta faixa etária. De acordo com um comunicado das empresas, o resultado do estudo deve ser conhecido nos próximos meses.
“Em última análise, acreditamos que três doses da vacina serão necessárias para crianças de 6 meses a 4 anos de idade para assim alcançarmos altos níveis de proteção contra atuais variantes e futuras potenciais. Se duas doses forem autorizadas, os pais terão a oportunidade de iniciar uma série de vacinação COVID-19 para seus filhos enquanto aguardam a possível autorização de uma terceira dose”, disse Albert Bourla, presidente e diretor executivo da Pfizer, em nota.
Anúncios
Teste da terceira dose
Em dezembro, Pfizer e BioNTech anunciaram que irão testar a terceira dose da vacina em crianças nesta faixa etária. A necessidade de avaliar uma 3ª dose surgiu após testes clínicos de fase 1, 2 e 3 revelarem que, em crianças entre dois e quatro anos, a resposta imune gerada foi mais fraca do que o esperado.
“A decisão de avaliar uma terceira dose de 3 µg para crianças de 6 meses a 5 anos reflete o compromisso das empresas em selecionar cuidadosamente a dose certa para maximizar o perfil de risco- benefício”, informou o laboratório.
Ao todo, participaram dos testes clínicos iniciais cerca de 4,5 mil crianças com idade de 6 meses a 12 anos de diversos países. Com exceção da faixa etária entre dois e quatro anos, a vacina de dosagem baixa (3 µg) foi capaz de ativar a resposta imune pretendida pela farmacêutica.
Os novos testes clínicos focados na terceira dose devem começar em janeiro e terão como objetivo avaliar a segurança, tolerância e capacidade do imunizante gerar proteção contra a doença. A terceira dose será administrada ao menos dois meses depois de completado o esquema vacinal primário (duas doses).
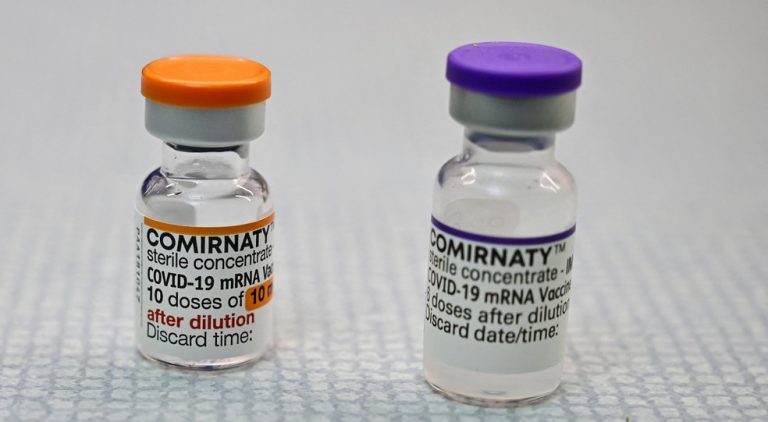
A vacina da Pfizer contra a Covid-19 tem registro para uso tanto em adultos como em crianças, o que diferencia é a dosagem. Para maiores de 12 anos deve ser utilizado a dosagem de 30 µg (frasco roxo) por vacina, enquanto que o público de cinco a 12 anos deve receber 10 µg (fraco laranja) do imunizante.
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2021/5/w/cRcJ3pSKeCLQ0EpqlSqQ/000-9um6vz.jpg)
Fonte: G1